Ministro de Salud y acuerdo con laboratorio chino por vacuna: “Si vamos a participar en el estudio, queremos que se nos asegure ese aporte”
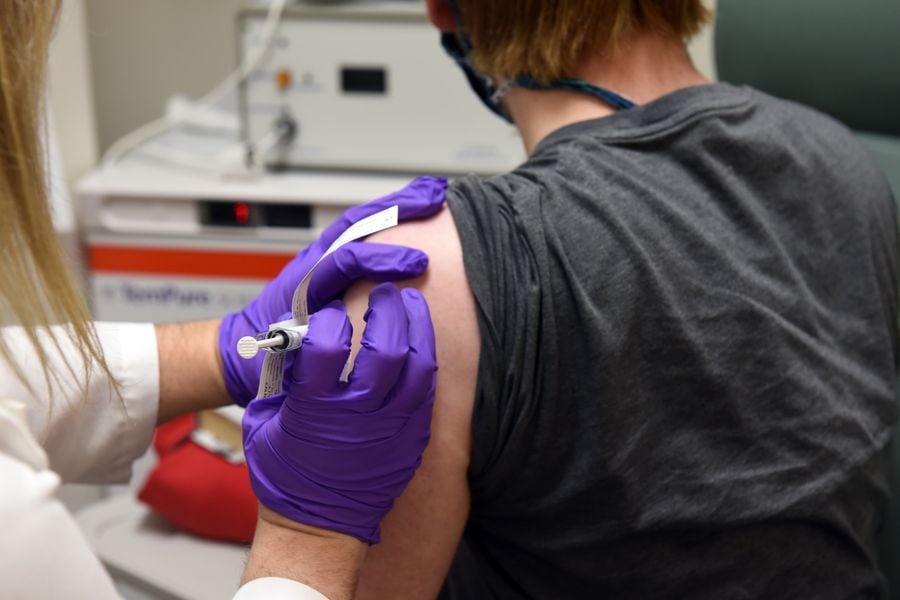
Enrique Paris aseguró que la idea es hacer pruebas clínicas en Fase 3, para lo que se requieren 3 mil personas y una considerable inversión de dinero. "Pensamos que al menos necesitamos 10 millones de vacunas para la población chilena", sostuvo.
El ministro de Salud, Enrique Paris, se refirió hoy al acuerdo del Gobierno con la empresa farmacéutica CanSino Biologics, quien anunció hoy que realizará pruebas en Fase 3 para las vacunas contra el Covid-19 en Chile.
“La propuesta de los laboratorios para acceder a la posibilidad de ensayos clínicos en Chile ha sido aceptada por el Gobierno. El presidente Piñera dio esa instrucción y estamos trabajando en conjunto con el Ministerio de Ciencias”, afirmó Paris. “La idea es hacer pruebas clínicas en Fase 3 para lo cual se requieren 3 mil personas y una considerable inversión de dinero”, agregó.
“Hay otras empresas que también están presentando propuestas para ensayos clínicos con vacunas y las tomaremos en consideración. Esto se evalúa con el comité de expertos, el Ministerio de Ciencias y tendremos que elegir la mejor posibilidad, la más beneficiosa, y que además nos permita obtener una cantidad importante de vacunas para la población”, dijo el Ministro.
“Pensamos que al menos necesitamos 10 millones de vacunas para la población chilena, y si vamos a participar en este estudio queremos que se asegure ese aporte”, sostuvo.
Asimismo, Paris recordó que “cuando una persona se enferma, produce anticuerpos activos que duran aparentemente poco tiempo; por otro lado, cuando alguien se vacuna, produce anticuerpos pasivos que defienden por más tiempo al paciente”
“Si logramos tener una vacuna, lograremos controlar de mejor forma la pandemia”, indicó.
Fase 3
En relación a la Fase 3 de la vacuna, la Dra. Sofía Salas, docente investigadora del Centro de Bioética, Facultad de Medicina de la Clínica Alemana-Universidad del Desarrollo, explicó que en esta etapa “el fármaco es administrado a miles de personas, en distintos lugares del mundo (multicéntrico), con el objeto de evaluar eficacia y seguridad”.
“Una vez terminada con éxito esta etapa, la vacuna se registra y puede ir a una Fase IV, en la que se registran los efectos de la vacuna en la administración ya en ambiente fuera de un ensayo clínico. Esto permite pesquisar eventos adversos poco frecuentes, aunque no siempre se hace un ensayo Fase IV para vacunas”, señaló.
“La medida de la eficacia de una vacuna se define por el porcentaje de reducción de la incidencia -de la enfermedad o de la infección- entre la población vacunada. Lo importante de esta etapa es que se prueba en las condiciones más reales posibles. Esta etapa es más larga, y puede llevar un año antes de tener resultados confiables”, asevera la especialista.

Comenta
Por favor, inicia sesión en La Tercera para acceder a los comentarios.