Ronapreve: todo lo que necesita saber del nuevo y prometedor tratamiento contra el Covid que acaba de ser autorizado
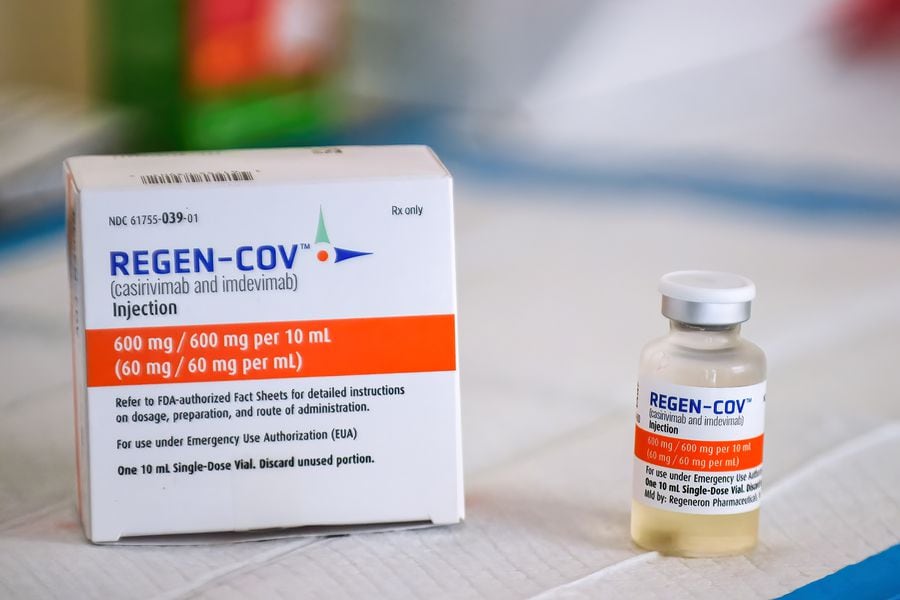
En octubre de 2020 fue utilizado por el presidente Donald Trump durante su infección por Covid-19. Desde entonces, ya tiene licencia para uso de emergencia en más de 20 países. Este es su verdadero poder para enfrentar la pandemia.
El regulador de medicamentos del Reino Unido acaba de aprobar un nuevo tratamiento contra el Covid-19. Con la marca Ronapreve en el Reino Unido y REGEN-COV en EE.UU., el medicamento fue desarrollado por Regeneron Pharmaceuticals junto a Roche. Primero ocupó los titulares en octubre de 2020 cuando el presidente Trump lo recibió durante su infección por Covid-19.
Ya tiene licencia para uso de emergencia en más de 20 países, incluidos EE.UU., Japón e India, y se usa para tratar o prevenir la infección aguda por Covid-19, aunque no sustituye a la vacuna. Administrado por inyección o infusión, está destinado a personas con alto riesgo de desarrollar Covid-19 grave. Se puede administrar a personas que ya muestran síntomas o a personas que han estado expuestas recientemente a alguien infectado para reducir el riesgo de contraer el virus.
Ronapreve pertenece a una clase de medicamentos llamados anticuerpos monoclonales o mAbs. Estas son moléculas producidas en un laboratorio que imitan los anticuerpos naturales que produce el sistema inmunológico para combatir las enfermedades.
¿Cómo actúa Ronapreve?
El tratamiento contiene dos mAbs: casirivimab e imdevimab. Están diseñados para evitar que el coronavirus se adhiera a ACE2, un receptor que se encuentra en la superficie de las células humanas en el tracto respiratorio. El virus se une al receptor para ingresar a la célula, donde puede replicarse antes de infectar otras células.
Uno de los mAb se deriva de una célula inmunitaria que combate el Covid extraída de un superviviente humano de la enfermedad. El otro se produjo en un ratón modificado genéticamente para tener un sistema inmunológico humano. La ventaja de combinar los dos es que se dirigen a dos partes diferentes de la proteína de pico, muchas de las cuales sobresalen del coronavirus; esto es lo que usa para unirse con ACE2. El uso de ambos reduce la posibilidad de que el virus se escape del sistema inmunológico.

El efecto del tratamiento es estimular la inmunidad de una persona, permitiendo que su respuesta inmune elimine el virus para que pueda recuperarse de la infección. En este sentido, funciona de manera similar a la terapia con plasma de convalecencia, en la que los anticuerpos de las personas que se han recuperado de una enfermedad se extraen de su sangre y se administran a otras personas para aumentar su capacidad de combatir la enfermedad.
Sin embargo, la ventaja de los mAb es que todos son idénticos y, por lo tanto, solo se unen al coronavirus en sí. Por lo tanto, tienen menos posibilidades de causar efectos secundarios que el plasma sanguíneo, que contiene una mezcla de anticuerpos que pueden unirse (y dañar) a otras células dentro del cuerpo.
¿Qué tan efectivo es este tratamiento?
Ronapreve se ha sometido a una serie de ensayos clínicos en todo el mundo. Según Regeneron, en julio de 2021, 16.000 pacientes, tanto en entornos hospitalizados como no hospitalizados, habían recibido el fármaco en ensayos. Los ensayos se dividen en etapas, y la etapa final, la fase 3, involucra a muchas personas para confirmar que el medicamento que se está probando funciona contra la enfermedad a la que se dirige.
Un estudio de fase 3 involucró a 1.505 participantes en EE.UU., Rumania y Moldavia. Todos habían estado expuestos a un contacto doméstico diagnosticado con Covid-19 en las últimas 96 horas. La mitad recibió Ronapreve, la mitad un placebo. Aquellos en el grupo de Ronapreve tenían un 81% menos de probabilidades de contraer Covid-19 por contacto con su hogar que aquellos en el grupo de placebo, y en aquellos que estaban infectados, el medicamento redujo la duración de sus síntomas y la cantidad de tiempo que consumieron altas cantidades de virus en su cuerpo.
El fármaco también se evaluó en el ensayo de recuperación del Reino Unido, un proyecto de amplio alcance que ha probado varios tratamientos de Covid-19. Probó Ronapreve en 9.785 pacientes hospitalizados con Covid-19, y algunos recibieron atención estándar y alguna atención estándar, además del medicamento. Entre los pacientes que en el momento de inscribirse no habían montado su propia respuesta de anticuerpos al virus, el fármaco redujo las muertes en una quinta parte.
Y otro estudio de fase 3 (actualmente todavía en preimpresión, por lo que espera la revisión de otros científicos), que involucró a pacientes hospitalizados de alto riesgo, sugiere que el medicamento reduce la hospitalización o muerte en un 70% y la duración de los síntomas en cuatro días.
¿Quién recibirá Ronapreve?
Es probable que esta terapia sea más beneficiosa para las personas con sistemas inmunitarios comprometidos, como las personas con VIH y cáncer, pacientes trasplantados que toman medicamentos inmunosupresores y aquellos con trastornos de inmunodeficiencia. Estas personas no solo son muy susceptibles a las infecciones, sino que también responden mal a la vacunación.
Sin embargo, queda por ver qué tan ampliamente se usa el tratamiento. Porque los anticuerpos son moléculas biológicas en lugar de químicas y solo pueden fabricarse en células de mamíferos en condiciones de laboratorio, lo que requiere mucho tiempo y es caro. Un gramo de mAb cuesta típicamente entre US $ 95 y US $ 200, sin incluir los costos de investigación.

Todavía no está claro exactamente cuál será el precio de Ronapreve. En India, una dosis cuesta £ 57.750 (más de medio millón de pesos), un precio que puede ponerla fuera del alcance de la mayoría del mundo. En EE.UU., sin embargo, está disponible sin cargo para las personas como parte de un programa financiado por el gobierno. Los expertos del Reino Unido recomiendan que el medicamento se reserve para los más vulnerables, ya que podría costar entre £ 1,000 y £ 2,000 por uso.
Por qué su aprobación es significativa
La técnica para producir mAb fue desarrollada por primera vez en el Reino Unido por César Milstein y Georges Köhler en 1975. Desde entonces, se han autorizado más de 100 medicamentos mAb en Europa y Estados Unidos para múltiples afecciones, y la tasa de aprobaciones aumenta rápidamente.
Sin embargo, hasta ahora solo se han aprobado unos pocos mAbs para enfermedades infecciosas. La mayoría se utilizan para tratar el cáncer y los trastornos autoinmunitarios . El progreso en el desarrollo de estos tratamientos para las enfermedades infecciosas ha sido lento, en parte debido a la continua alta dependencia de los antibióticos, que son más baratos de producir y más fáciles de administrar a los pacientes. Otro factor limitante ha sido el hecho de que las enfermedades infecciosas tienden a ser de corta duración, por lo que sus tratamientos tienen un valor de mercado limitado. Esto ha dado a las empresas pocos incentivos para invertir en dichos medicamentos.
Entonces, además de ofrecer una nueva forma de proteger a las personas del Covid-19, la autorización de un tratamiento de este tipo para esta enfermedad es un hito importante en el desarrollo de mAb.
* Investigador invitado, Historia de las Ciencias Biomédicas, Universidad de Cambridge

Comenta
Por favor, inicia sesión en La Tercera para acceder a los comentarios.