Ahora Janssen: ISP revisará mañana quinto permiso de una vacuna contra el Covid-19 y estaría disponible en julio
El fármaco del laboratorio Johnson&Johnson llegará al país de la mano del convenio internacional Covax, por lo que se homologará la autorización que ya le entregó la Organización Mundial de la Salud. Se trata de una monodosis que, a 28 días de su aplicación, ha reportado una efectividad del 85,4% frente a casos severos. Preliminarmente, se espera un primer envío superior a las 500 mil dosis.
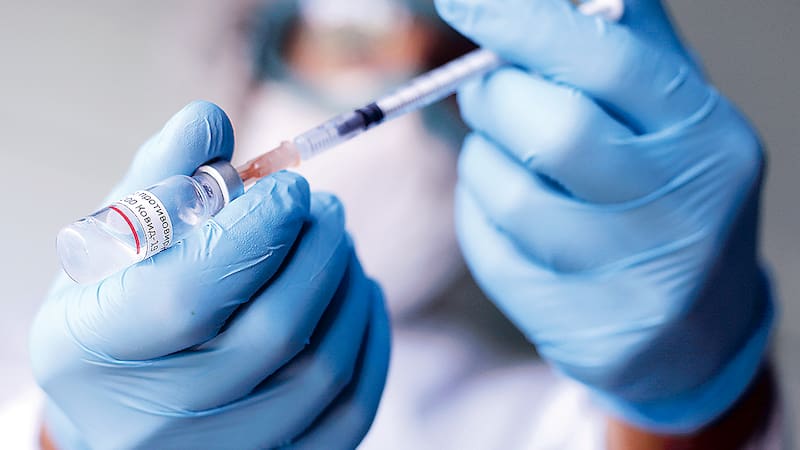
Para mañana, a contar de las 9.00, está programada la sesión del Instituto de Salud Pública (ISP) donde se revisarán los antecedentes de la vacuna Janssen del laboratorio norteamericano Johnson&Johnson, que está próxima a llegar al país de la mano del convenio internacional Covax, tal como ya ocurrió con las primeras dosis de Astrazeneca.
A diferencia de las audiencias previas, esta vez la validación del uso de emergencia del fármaco se realizará mediante una homologación del permiso que ya entregó la Organización Mundial de la Salud a la vacuna Janssen, para mayores de 18 años.
Al respecto, el director (S) del Instituto de Salud Pública, Heriberto García, explicó que la OMS tiene un comité internacional de expertos donde se realiza la precalificación de las vacunas, dentro del que participan dos funcionarios del ISP. Dicha instancia ya autorizó, en marzo pasado, el uso del antídoto norteamericano.
“Esta vacuna ya fue revisada por expertos internacionales, entonces hacer acá, nuevamente, la medición de eficacia y seguridad sería darnos una vuelta más, por lo que nosotros vamos a aprobarla también. Sabemos que durante el segundo semestre la vacuna va a ingresar por el mecanismo Covax, entonces esto nos permite avanzar y que no perdamos tiempo cuando exista la posibilidad de traerla, y dejar pendiente solo la parte administrativa, que tiene que ver con el sitio de fabricación”, explicó García.
La vacuna de Johnson&Johnson es una monodosis intramuscular que ya ha sido autorizada en Brasil, Reino Unido, Canadá, Estados Unidos, México, Colombia y en la Unión Europea, para personas mayores de 18 años.
De acuerdo a los datos reportados, Janssen tiene una eficacia general del 66,9% a los 14 días de haber sido suministrada. Para casos severos o críticos, en tanto, su cobertura se empina al 76,7% a las dos semanas, y sube al 85,4% en los 28 días posteriores a su inoculación.
García, eso sí, explica que no se descarta que las personas puedan requerir, a futuro, una nueva dosis. “Se ha visto que en las personas que cursan la enfermedad alrededor del cuarto mes empiezan a bajar los anticuerpos en forma importante, mientras que con las otras vacunas empiezan a bajar al sexto mes; por eso se habla de la posibilidad de refuerzo. Pero no está completamente estudiada aún la inmunidad celular histórica, por llamarla así, que tiene el cuerpo. Es como con las vacunas que nos pusimos de niños, actualmente no tenemos ningún anticuerpo en la sangre, pero tenemos la respuesta suficiente y nuestro ADN ya sabe que si entra un virus de esa enfermedad debemos producir inmediatamente el anticuerpo necesario para evitar enfermarnos”, explica García
El uso de la vacuna de Johnson&Johnson, tal como ha ocurrido con la de AstraZeneca, ha sido suspendido en algunos países tras la aparición de casos de trombosis. Sin embargo, tanto la Agencia Europea del Medicamento (EMA) como la Agencia de Medicamentos de Estados Unidos (FDA) respaldaron la continuación de su uso.
“Es una muy buena noticia que el ISP revise los antecedentes de la vacuna de la compañía Janssen, que consiste en un vector adenoviral contra Covid-19 que ya ha sido probado en más de 44 mil personas en ensayos clínicos, donde ha participado también Chile. Se ha mostrado una eficacia del 72% para prevenir la infección y tiene la ventaja de que es de una sola administración. Esto viene a aumentar la variedad de alternativas que tenemos para vacunar a nuestra población”, planteó Carlos Pérez, infectólogo de Clínica Universidad de los Andes y decano de la Facultad de Medicina y Ciencia de la Universidad San Sebastián.
De acuerdo a las conversaciones que se han sostenido a la fecha, en el Ministerio de Salud prevén que las primeras dosis lleguen durante el próximo mes, con un primer envío de casi 500 mil unidades. Así, Janssen se transformaría en la quinta vacuna en estar disponible en el país, lo que permitirá reforzar la estrategia de inmunización que, en las próximas semanas, abordará a un nuevo grupo etario: los menores de entre 12 y 16 años, con la vacuna de Pfizer.
Al respecto, el académico de la Usach Claudio Castillo plantea que “la estrategia de compra que ha usado Chile ha sido diversificada y colaborativa. Se ofreció a distintos laboratorios desarrollar ensayos clínicos en el país, siendo cuatro: Sinovac con la Universidad Católica, Oxford-AstraZeneca y Janssen con la Universidad de Chile y CanSino con la Universidad de la Frontera, todos con una red de centros de salud pública y privados que estaban conectados, disponibles, para hacer las conexiones con los potenciales voluntarios. Por lo tanto, hubo una oferta de colaboración y de facilidades para el desarrollo de ensayos clínicos a cambio de contratos que priorizaran el país”. En paralelo, agregó el académico, “el gobierno ha informado convenios con Sinovac, Pfizer-Biontech, Oxford-Astrazeneca, Janssen, CanSino y Covax, y señalado que hay negociaciones con Sinopharm, Serum Institute de India y el Instituto Gamaleya de Rusia por Sputnik V”.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
La mayoría no entiende el debate por el impuesto a las empresas. El resto lee La Tercera.
Plan Digital+$6.990 al mes SUSCRÍBETE