ISP autoriza uso de emergencia de Sputnik V y se convierte en la sexta vacuna aprobada en Chile
Hasta ahora, las vacunas aprobadas por el Instituto de Salud Pública corresponden a cinco laboratorios: Pfizer BioNTech, Sinovac Biotech, AstraZeneca, CanSino y Janssen.
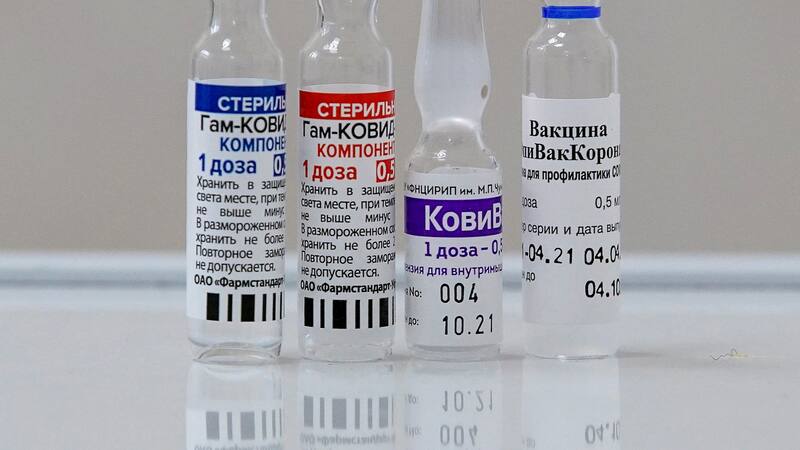
El Instituto de Salud Pública (ISP) y el Comité de Expertos convocado para esta decisión, aprobaron con 5 votos a favor, dos abstenciones y un rechazo, el uso de emergencia de la vacuna Sputnik V, lo que la convierte en la sexta herramienta de inmunización contra el Covid-19 autorizada en Chile.
La vacuna del laboratorio ruso Gamaleya fue aprobada para su uso en mayores de 18 años, pero no en embarazadas, mujeres en periodo de lactancia, ni personas con problemas inmunes ya que no se han realizado estudios clínicos sobre estas poblaciones. Tras la discusión, que no pudo ser transmitada en su totalidad debido a problemas técnico, concluyó que la vacuna es segura pero solicitaron más antecedentes, específicamente sobre los estudios de inmunogenicidad.
El director (s) del ISP, Heriberto García, dijo desde hace más de dos meses que se estaban revisando y evaluando los antecedentes de esta vacuna. Sobre el voto de rechazo y las abstenciones, indicó que los tres fueron similares “desde el punto de la neceisdad de que existan mayores antecedentes con respecto a la duración de la eficacia de esta vacuna, principalmente porque en los estudios clínicos de la vacuna se midió la inmunogenicidad al día 42 y de ahí no se han tenido mayores resultados a diferencia de otros estudios clínicos en los que se ha ido avanzando y sabiendo que la inmunidad dura más tiempo”.
Ya en septiembre de 2020, el Ministerio de Ciencia, a través de su Consejo Asesor de Vacunas, había mostrado interés en esta vacuna cuando participó en una videoconferencia con los representantes de los ministerios rusos a cargo del desarrollo y comercialización de Sputnik V. Lo que buscaba la cartera en esa oportunidad era conseguir la realización de ensayos clínicos en Chile y evaluar la tecnología que se estaba desarrollando.
¿Cómo funciona? Esta vacuna utiliza dos adenovirus humanos modificados que en su interior lleva consigo un gen que codifica la proteína Spike o S del nuevo coronavirus. En la primera dosis se utiliza un adenovirus que actúa como vehículo de la proteína y en la segunda otro. A la fecha, los estudios muestran una eficacia superior al 90%.
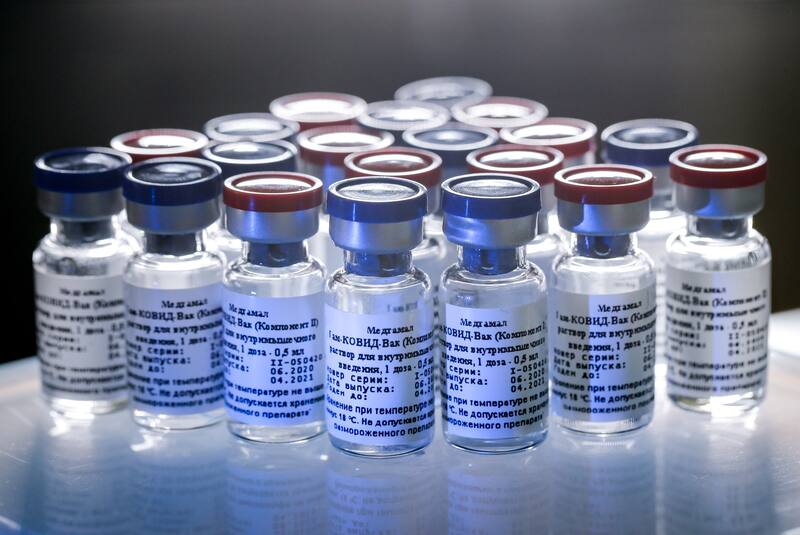
Respecto de su almacenamiento, solo necesita una refrigeración similar a la mayoría de las vacunas (entre 2 y 8°C).
Los efectos adversos reportados en la población que ya se está vacunando con ella, como México y Argentina, son menores y hasta ahora no se han registrados notificaciones de preocupación.
Según los antecedentes presentados para su aprobación, más del 99% de los eventos reportados por quienes fueron inoculados en el estudio clínico con esta vacuna, se clasificaron como leves y moderados (no serios), mientras que el evento reportado con mayor frecuencia fueron síntomas similares a un cuadro de resfrío común. Estos efectos adversos, se presentaron el primer o segundo día tras la inmunización y, generalmente, disminuyeron dentro de los tres días siguientes.
De acuerdo a un estudio dado a conocer por The Lancet en noviembre pasado, la vacuna cuenta con un 91% de eficacia y seguridad para adultos mayores. En abril de este año, en tanto, el Centro Nacional de Investigación de Epidemiología y Microbiología Gamaleya del Ministerio de Salud de la Federación Rusa y el Fondo de Inversión Directa de Rusia (RDIF), anunciaron la efectividad de la vacuna en un 97,6%, según el análisis de datos sobre la incidencia de coronavirus entre los rusos vacunados con ambos componentes del fármaco.
Actualmente, esta vacuna se utiliza en más de 70 países entre ellos Argentina, Brasil, México y Hungría. Los estudios realizados en mayores de 18 año y también mayores de 60 años, consideran la eficacia a los 21 días después de la segunda dosis.
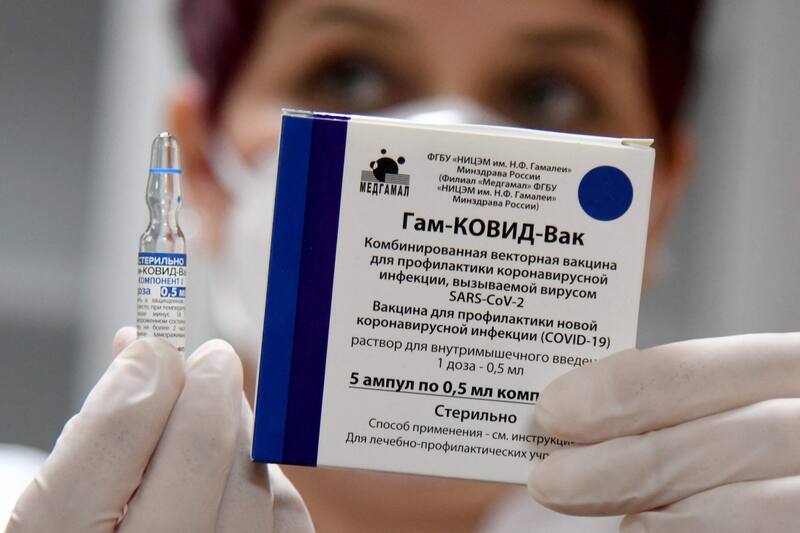
Si bien no existe claridad respecto de la cantidad de dosis que el gobierno negoció con el Instituto Gamaleya en febrero pasado el embajador de Rusia en Chile, Sergei Koshkin, señaló que podrían ser hasta ocho millones. Sin embargo, en marzo, el subsecretario de Relaciones Económicas, Rodrigo Yáñez, precisó que se discutía la posible llegada entre tres a cuatro millones.
Hasta ahora, las vacunas aprobadas por el Instituto de Salud Pública corresponden a cinco laboratorios: Pfizer BioNTech aprobada en diciembre del año pasado; Coronavac de la farmacéutica china Sinovac Biotech con autorización desde enero de este año; la vacuna desarrrollada por el laboratorio farmacéutico británico AstraZeneca y la Universidad de Oxford autorizada a fines de enero; Convidicea del laboratorio chino canadiense CanSino aprobada a comienzos de abril; y la recien autorizada a comienzos de este mes, la vacuna de la farmacéutica Janssen (laboratorio de Johnson & Johnson).
Incorporación positiva
Para el doctor José Gregorio Martínez, infectólogo de Clínica Vespucio, la incorporación de una nueva plataforma de vacunas es positiva, sobre todo, considerando “el momento en que estamos en la campaña de vacunación en Chile, donde se ha logrado la cobertura de un alto porcentaje de la población objetivo, y se ha visto la posibilidad de una tercera dosis, la incorporación de vacunas con diferentes tecnologías y de nuevos laboratorios siempre va a ser positiva porque eso amplía las posibilidades de vacunación en la población y permite tener un mayor número de dosis de refuerzo”.
Con respecto a la vacuna Sputnik V, el especialista señala que revistas científicas importantes han publicado resultados que revelan una eficacia cercana al 91% y eso cumple el requisito mínimo exigido por la Organización Mundial de la Salud (OMS). “No tendría por qué cuestionarse la eficacia de esta vacuna para incorporarla a la campaña de vacunación en Chile. Sí es cierto que esta vacuna no ha recibido la aprobación en algunos países, y algunos han reportado que se han encontrado adenovirus replicantes en alguno de los lotes”, reconoció.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Casi nadie tiene claro qué es un modelo generativo. El resto lee La Tercera.
Plan Digital + LT Beneficios$6.990 al mes SUSCRÍBETE











