Chile inicia las pruebas para una vacuna contra el coronavirus
Este mediodía, el ministro de Salud, junto a autoridades del Instituto de Salud Pública y la U. de Chile y U. Católica, dieron a conocer los detalles del comienzo de estas pruebas. Tres laboratorios ya han solicitado formalmente al ente regulador la autorización para dar comienzo a estos ensayos, dos fueron autorizados.
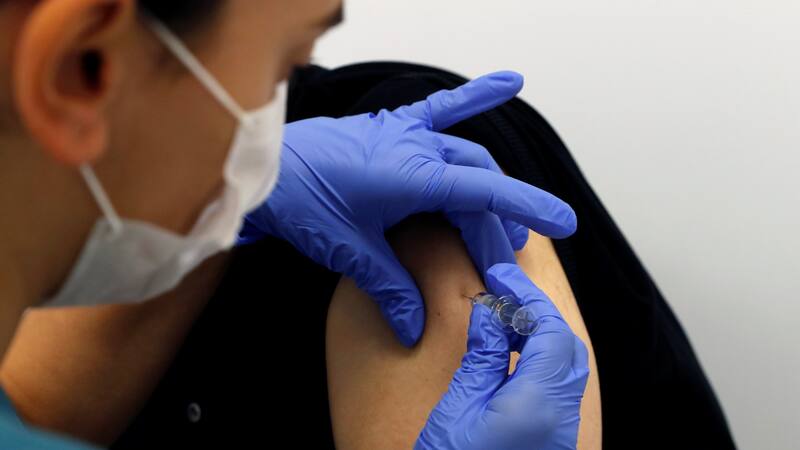
Desde el inicio de la pandemia por coronavirus, la ciencia y la medicina se volcaron el búsqueda de una vacuna para poder combatir este patógeno.
Desde entonces, se han desarrollado 191 prototipos de vacunas (41 en fases clínicas en humanos), según la última actualización de la Organización Mundial de la Salud (OMS), algunos en estados tan avanzados, que ya se encuentran en pruebas de fase 3, la última fase en humanos, en la que se prueban masivamente para medir eficacia y seguir midiendo seguridad.
Tres de las más prometedoras se probarán en Chile: la que desarrolla el laboratorio Jannsen, la que está produciendo su par chino Sinovac y la de AstraZeneca junto a la U. de Oxford.
Las tres pruebas estaban esperando la autorización del Instituto de Salud Pública (ISP), institución que tal como informó Qué Pasa el 15 de septiembre, había creado un comité de ética para aprobar estas pruebas.
Este mediodía, el ministro de Salud, Enrique Paris, junto al director (s) del Instituto de Salud Pública, Heriberto García, dieron a conocer la autorización para los dos primeros ensayos: Sinovac Biotech y Janssen Pharmaceutical Companies.
Cada uno de ellos podrá probar vacuna candidata en 3.000 voluntarios.
En la actividad también estuvo presente el rector de la Universidad de Chile, Ennio Vivaldi; el rector de la Universidad Católica, Ignacio Sánchez, además del académico e investigador del Instituto de Ciencias Biomédicas de la Facultad de Medicina de la Universidad de Chile, Miguel O’Ryan y el director del Instituto Milenio en Inmunología e Inmunoterapia, Alexis Kalergis.
El director (S) del ISP, Heriberto García, señaló que la autorización se concretó luego de que se evaluaran las solicitudes para el uso en investigación de estas vacunas candidatas, lo que también implicó la revisión de los protocolos de los ensayos clínicos, los manuales de los investigadores y los antecedentes de la fabricación de las vacunas, sus posibles reacciones adversas, así como el cumplimiento de las Buenas Prácticas Clínicas (BPC) y las Buenas Prácticas de Manufactura (BPM) de estos productos farmacéuticos destinados al uso en investigaciones científicas en seres humanos.
García destacó que una vez que importen las vacunas y estas lleguen a Chile, la farmacovigilancia, rol que está a cargo del ISP, en caso de que aparezcan reacciones adversas tras la inoculación. “El ISP es reconocido a nivel mundial como una agencia reguladora nivel 4, estamos al mismo nivel que la FDA y la EMA. Ellos también nos piden recomendaciones sobre el trabajo que nosotros estamos haciendo para replicarlo en sus países y eso me llena de orgullo”, aseguró.
Las vacunas que se probarán en Chile
La primera vacuna que anunció el inicio de pruebas en el país, fue la que desarrolla el laboratorio chino Sinovac, que logró un acuerdo con la U. Católica a través del Instituto de Inmunoterapia e Inmunología (IMII) que dirige Alexis Kalergis.
Luego se anunció que la vacuna que desarrollar el laboratorio Janssen (de la multinacional Johnson & Johnson), el que se realizará en algunos consultorios de San Bernardo y Colina, coordinados por la U. de Chile.
También se había anunciado que el prototipo que desarrolla el AstraZeneca junto a la U. de Oxford, también sería probada en el país, a través de un convenio con la Clínica las Condes y la U. de Chile donde estaría encabezado por la académica María Elena Santolaya.
Sin embargo, este ensayo aún no iniciaría sus pruebas ya que su aprobación está aún en proceso, pero según el director (s) del ISP, pronto se vendrán más autorizaciones.
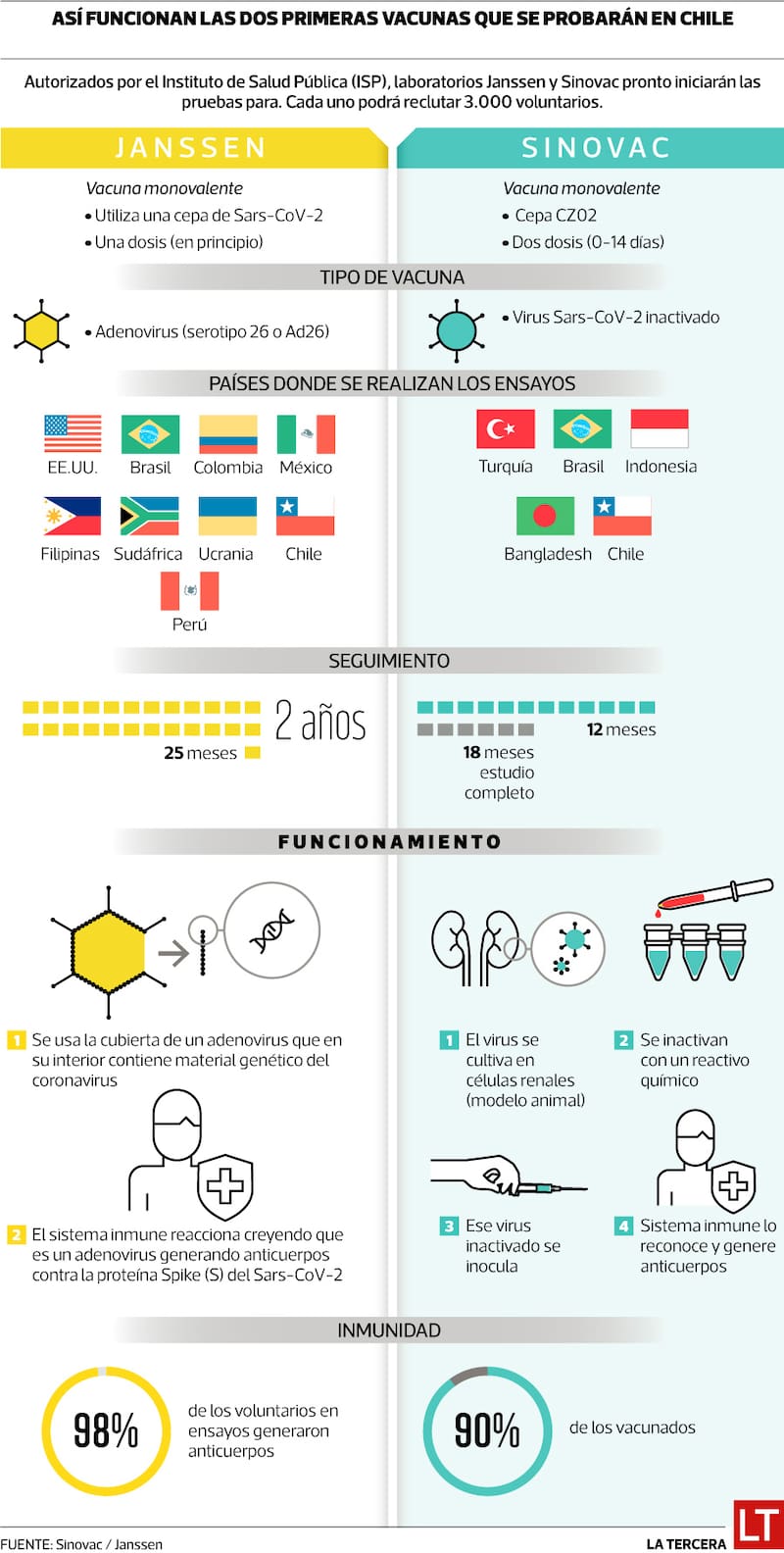
Ensayos autorizados
La Comisión de Estudios Clínicos del Instituto de Salud Pública de Chile (ISP) votó favorablemente la autorización de dos de los tres estudios clínicos en fase 3 que habían hecho la solicitud: Sinovac Biotech Co., Ltd. y Janssen Pharmaceutical Companies.
Esta comisión asesora al director del ISP, en la evaluación de los aspectos que otorguen las garantías suficientes de que haya un diseño adecuado del estudio, así como cumplimiento de las Buenas Prácticas Clínicas y otras guías internacionales, como también de la calidad de la vacuna en investigación.
Para el ensayo de la vacuna china Sinovac Biotech se autorizó su uso en pruebas de inmunización en la que participen hombres y mujeres entre los 18 y 59 años con la excepción de mujeres embarazadas, personas que ya hayan tenido Covid-19 y personas inmunodeprimidas.
Tal como había sido anunciado por los encargados del estudio, los primeros participantes serán trabajadores de la salud (que están más expuestos al virus) y luego se incorporarán otros voluntarios con alto riesgo de contagio.
El estudio de la vacuna de Janssen, liderado por la U. de Chile, también incluirá voluntarios entre los 18 y 59 años en una primera etapa y luego también sumará a adultos mayores.
Los dos ensayos están autorizados a incluir como voluntarios a personas con condiciones médicas crónicas (diabetes, hipertensión, obesidad, asma y fumadores) siempre que mantengan un control adecuado de ellas y no presenten descompensación.
Participantes
Considerando los dos ensayos, serán 6.000 voluntarios los que participarán. En cada uno de ellos, serán varias instituciones las que participarán en el enrolamiento y seguimiento.
El próximo paso es iniciar los trámites de importación de las vacunas y la búsqueda de las seis mil personas dispuestas a participar en los ensayos.
“Antes de la vacunación de toman muestras de sangre para ver los parámetros inmunológicos de la persona, y después de ser inmunizadas se sigue durante un par de semanas con un seguimiento de manera más intensa, para evaluar la reactogenicidad o respuesta a la vacunación en los distintos sub grupos. Las personas mantienen comunicación permanente con los equipos del estudio para analizar reacciones locales o sistémicas de la vacunación”, explica O’ Ryan.
En el caso del ensayo de la vacuna de Janssen, los participantes del ensayo, se enrolarán en los centros de salud familiar de Colina y San Bernardo, y el hospital Exequiel González Cortés, que son las otras entidades coordinadas por la U. de Chile. Una vez que las vacunas ya estén en Chile, la vacunación de todos los voluntarios debiera demorar entre 45 y 60 días (octubre y noviembre).
Susan Bueno, investigadora del IMII y directora científica del estudio que evaluará la vacuna china, explica que una vez que se cuente con toda la documentación del ISP que autoriza el ingreso de la vacuna a Chile, se podrá iniciar el proceso de importación. “Como la importación de un producto biológico implica una importante coordinación, no es posible anticipar una fecha exacta, pero debería iniciarse en las próximas semanas", adelanta.
Respecto de los participantes, Bueno señala que ya están en la etapa de preparación del estudio, en la que se está realizando toda la coordinación en los centros de investigación que participarán en este estudio para iniciar la ejecución. “Esto significa, entre otros aspectos, el enrolamiento de los voluntarios. Se contará con la colaboración de al menos nueve centros de Santiago y regiones, los que podrán iniciar el reclutamiento una vez que, entre otras etapas, las vacunas ya hayan sido importadas”.
En una primera etapa, el estudio de Sinovac, solo incorporará a personal de salud, con posibilidades que más adelante se pudiera incluir público general. “El reclutamiento si iniciará en las próximas semanas y a través de los canales de comunicación formal de la UC, se informará cuándo”, dice.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
Casi nadie tiene claro qué es un modelo generativo. El resto lee La Tercera.
Plan Digital + LT Beneficios$6.990 al mes SUSCRÍBETE













