Vacuna de Pfizer podría ser autorizada a partir de la próxima semana en Chile
ISP y comité de expertos que revisarán los antecedentes presentados por el laboratorio, podrían aprobar su uso en una reunión a realizarse entre el 10 y el 18 de diciembre.
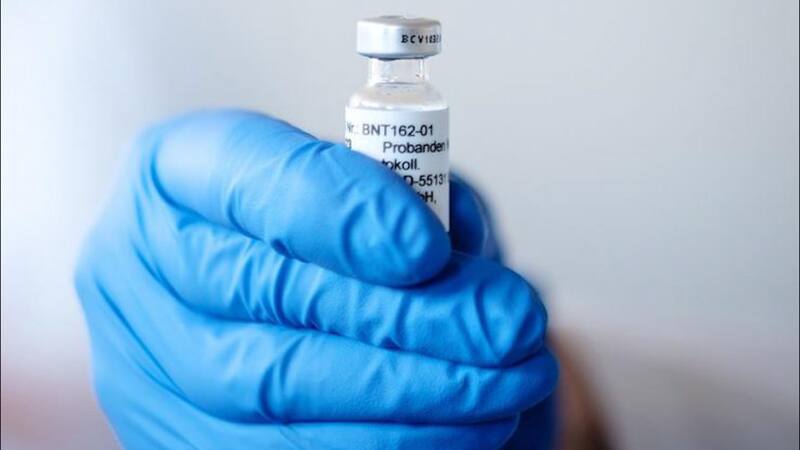
Para la autorización de uso especial que requiere la vacuna de la farmacéutica Pfizer y BioNTech, el Instituto de Salud Pública (ISP) llamó a un comité de experto para que asesore a esta agencia reguladora en esta decisión.
Lo mismo ocurrirá en Estados Unidos. La compañía quiere que su prototipo de vacuna comience a ser utilizado en la prevención de Covid-19 antes de terminar los estudios clínicos, tras los excelentes resultados preliminares obtenidos a la fecha (95% de efectividad), presentó los documentos para una aprobación de emergencia, decisión para la que la agencia de Administración de Medicamentos y Alimentos (FDA, su sigla en inglés) , también solicitó la conformación de un grupo de expertos.
Este jueves 10 de diciembre, será el día elegido para la decisión estadounidense y siete días más tarde, los mismo expertos decidirán respecto de la vacuna de la compañía Moderna, la otra farmacéutica que presentó sus documentos para una autorización de este tipo.
En Chile, la reunión entre los expertos del consejo asesor y los especialistas del ISP que decidirá si autoriza o no su uso en el país, ocurrirá entre el 10 y el 18 de diciembre, tal como lo adelantó el directo (s) de esta institución Heriberto García Escorza.
Por ahora, explicó García, no hay una fecha exacta, porque deben coordinar horarios entre 22 personas, pero cree que la resolución será rápida y que una sesión será suficiente.
De aprobarse, el trabajo del ISP no termina ahí. Se debe considerar que las vacunas para Covid-19, tendrán también un control previo, mediante Control de Serie, proceso mediante el cual se revisará, lote a lote, el protocolo de producción y control de calidad, así como sus certificados de liberación y condiciones de transporte, mediante una revisión documental.
“Todos los medicamentos y vacunas están sujetos a fiscalización y vigilancia”, dice García. El otorgamiento del registro sanitario, añade, impone obligaciones al titular respecto a la vigilancia del producto (detección y reporte de reacciones adversas), a la vez que el ISP, dentro de sus funciones de control de los medicamentos, incluye la fiscalización (de que todo el proceso de internación, distribución y uso de la vacuna se está haciendo conforme a la autorización concedida) y vigilancia de efectos adversos.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
Casi nadie tiene claro qué es un modelo generativo. El resto lee La Tercera.
Plan Digital + LT Beneficios$6.990 al mes SUSCRÍBETE