Todo lo que sabemos de CanSino, la vacuna de una dosis que solicitó autorización para ser usada en Chile
La vacuna con el ensayo más grande en el país cuenta con alta efectividad, la ventaja de una sola dosis y refrigeración normal, a diferencia de otros fármacos. La resolución del ISP sobre su uso vendrá en las próximas semanas, aunque ya existe un preacuerdo con 1,8 millones de dosis para el segundo semestre de este año.
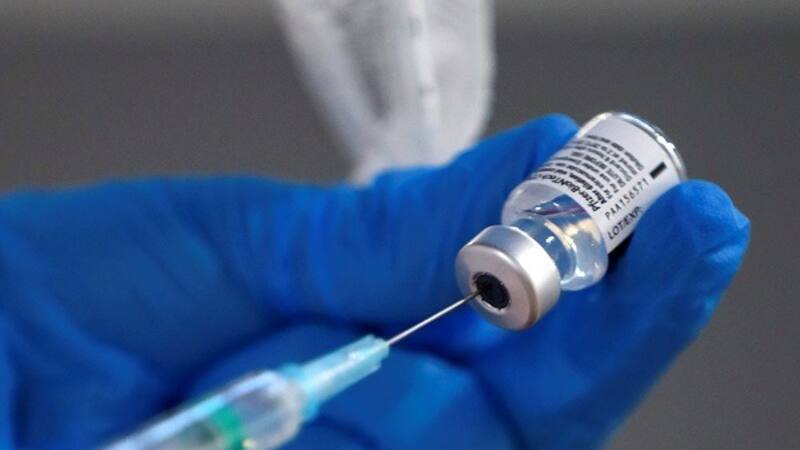
El 2 de diciembre de 2020 fue un mes crucial en la lucha contra el coronavirus en Chile. Ese día, la empresa chino/canadiense CanSino se sumó a los laboratorios Sinovac, Oxford y Janssen en las pruebas Fase III en el país, última antes de su distribución masiva y que tiene como objetivo evaluar la efectividad del medicamento en poblaciones masivas. Hoy, más de tres meses después y con promisorios resultados sobre la mesa, CanSino anunció, junto al laboratorio Saval, la solicitud ante el Instituto de Salud Pública (ISP) del registro de emergencia para la importación y distribución en el país de su vacuna contra el coronavirus, evaluación que debiese ser realizada por el ISP en abril próximo, según anunció este jueves el ministro de Salud, Enrique Paris.
“Las conversaciones comenzaron hace varios meses”, dice Nicolás Donoso, gerente general de Saval. “Desde el principio estuvimos siguiendo la estrategia de inmunización implementada por el Gobierno y gracias a nuestra experiencia en la producción y distribución de fármacos, se nos presentó la oportunidad de participar en las gestiones para representar a la vacuna de CanSino en Chile. El rol que ha tenido el país en los ensayos clínicos de Fase III, liderados por la Universidad de la Frontera, fue también clave para lograr un acuerdo para la provisión oportuna de vacunas para el país”, comenta, añadiendo que el preacuerdo implicaría la llegada de 1.800.000 dosis para el segundo trimestre de este año.
La vacuna, desarrollada por CanSino, el Instituto de Biotecnología de Beijing y la Academia de Ciencias Médicas Militares, es una vacuna de vector viral similar a la de AstraZeneca y Gam-COVID-Vac de Gamaleya, esta última desarrollada en Rusia. Para su elaboración, CanSino trabajó en una plataforma de adenovirus tipo 5, el cual ya fue probado en una vacuna desarrollada para combatir el virus del ébola. Las pruebas de fase I y II se reportaron seguras y con buena respuesta inmune. Llamada Convidicea (de nombre científico Ad5-nCoV) tiene una muy buena eficacia: los resultados preliminares del estudio Fase III mostraron un 91% para prevenir casos graves y un 65% para a evitar los casos sintomáticos de coronavirus.
“Esta eficacia además ha sido testeada en Chile a través de estudios liderados por la Universidad de La Frontera en conjunto con las universidades Austral y San Sebastián, además de centros de investigación de las ciudades de Santiago, Temuco, Valdivia, Osorno y Puerto Montt”, sostiene Nicolás Donoso.
Además de Chile, la vacuna de CanSino fue probada en más de 42 mil voluntarios de Pakistán, Rusia, China, México y Argentina, aunque en Chile fue el estudio fase 3 más masivo de todos, con cerca de 3.500 voluntarios.
En relación a las características más notables de la vacuna, ésta se aplica en una sola dosis, lo que simplifica y acelera la inoculación. Además, tiene una logística más sencilla debido a que requiere de una refrigeración entre 2° y 8° grados, a diferencia de fármacos que requieren de temperaturas más frías, o de dos dosis para entregar una protección más alta.
El Dr. Fernando Lanas, académico de la Universidad de La Frontera e investigador que lidera el estudio de Fase III de la vacuna CanSino en Chile, cuenta que “se hizo el análisis con los primeros 101 casos de Covid y de ahí salieron los datos de efectividad. El estudio cerró el enrolamiento con 42 mil personas aproximadas y se hará el segundo análisis con 150 casos de Covid, pero todos los ensayos clínicos siguen por seguridad hasta cumplir un año”.
“La evaluación es muy positiva. Estamos como universidad e investigadores muy contentos, ya que los 3.500 voluntarios involucrados en el estudio son el numero más grande de personas en un ensayo clínico de cualquier índole. Por el lado de los resultados, fueron los esperados: buena seguridad y una efectividad bastante razonable, similar a la vacuna de Janssen aprobada por autoridades sanitarias de Estados Unidos”, dice.
“Por cierto, es más fácil vacunarse una vez que dos veces, y para personas que les cuesta este trámite será más sencillo; además, desde el punto de vista geográfico también es un gran aporte en términos de armar equipos y llevar vacunas”, afirma Lanas.
“Estoy muy satisfecho por cómo se hizo el proceso y que el Ministerio de Ciencias haya tenido la visión de poner a Chile como uno de los países que participaron del ensayo, esperando a su vez que el ISP apruebe la autorización y la disponga para todos los chilenos”, sostiene Lanas.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
Casi nadie tiene claro qué es un modelo generativo. El resto lee La Tercera.
Plan Digital + LT Beneficios$6.990 al mes SUSCRÍBETE













