Variantes del Covid: el arduo trabajo científico para lograr una única vacuna para vencerlos a todos
Científicos en todo el mundo corren una maratón para desarrollar una inyección global capaz de detener todas las variantes del Sars-CoV-2 y anticiparse a futuras pandemias.
El Sars-CoV-2, el virus responsable del Covid-19, ha puesto al mundo patas arriba. Los expertos han predicho que se cobrará la vida de entre 9 y 18 millones en todo el mundo. Esto se suma a la destrucción de los medios de vida, la salud mental y la educación de muchos otros. La pandemia probablemente causará estragos durante muchos años, a pesar de la notable velocidad de desarrollo de la vacuna. Esto no se ve ayudado por la aparición de nuevas variantes que se extienden por todo el mundo, que representan una seria amenaza para el éxito de la vacunación y los próximos tratamientos.
Es difícil predecir el patrón futuro del Sars-CoV-2. Muchos científicos creen que seguirá circulando por todo el mundo, lo que significa que se volverá endémico de la misma forma que la gripe. En este contexto, el número de infecciones se mantiene relativamente constante con brotes ocasionales que corren el peligro de convertirse en una pandemia. Mucho depende de cuán ampliamente se pueda vacunar la población de todo el mundo y cuánto tiempo dure la inmunidad después de la infección natural o la vacunación.
A largo plazo, la mejor solución sería desarrollar una vacuna universal, una que ayude a proteger contra todas las variantes actuales del coronavirus y cualquier otra que surja en el futuro. Sin él, el mundo corre el riesgo de sufrir pandemias recurrentes.
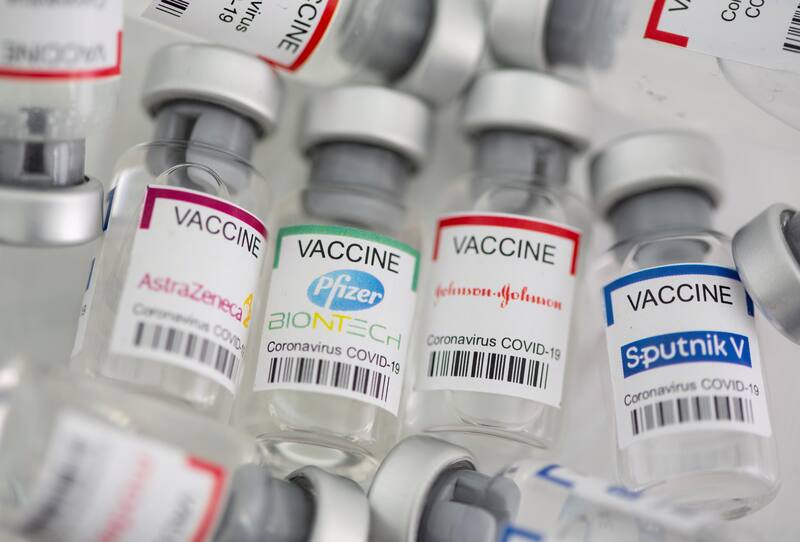
Dadas las dificultades encontradas para crear una vacuna universal contra la gripe, esto puede parecer una tarea difícil. Pero varios científicos creen que es posible basándose en el rápido desarrollo de las vacunas contra el Sars-CoV-2.
Covid-19 es, de hecho, el tercer brote importante de enfermedades infecciosas que se ha desencadenado en las últimas dos décadas por un nuevo coronavirus que salta de animales a humanos, los otros dos son Sars y Mers.
Para tener una idea de hasta qué punto ha progresado una vacuna contra el pan-coronavirus, hablamos con varios científicos claves en este campo. Todos son expertos en esta área, pero lo abordamos desde ángulos muy diferentes: Lara Marks es una historiadora de la medicina interesada en la biotecnología y las vacunas, mientras que Ankur Mutreja tiene experiencia en el seguimiento de brotes y el desarrollo de vacunas para enfermedades infecciosas. A partir de nuestras conversaciones, parece haber una serie de vacunas candidatas alentadoras en el horizonte; incluso es posible que se pueda desarrollar una para su uso en humanos dentro de los 12 meses.
El Santo Grial
Una de las primeras personas con las que hablamos fue Richard Hatchett , director ejecutivo de Coalition for Epidemic Preparedness Innovations (Cepi). Establecida en 2017, Cepi es una asociación global entre organizaciones públicas, privadas, filantrópicas y de la sociedad civil que tiene como objetivo comprimir el desarrollo de vacunas contra enfermedades infecciosas emergentes en 100 días, un tercio del tiempo logrado con las primeras vacunas Covid-19.
Con la visión de un acceso equitativo a las vacunas para todos los países, en marzo de 2021, Cepi anunció que recaudaría e invertiría US $ 3,5 mil millones en investigación y desarrollo de vacunas para fortalecer la preparación mundial para las pandemias, de los cuales US $ 200 millones se han reservado para desarrollar una vacuna universal contra el coronavirus. Una vacuna de este tipo ofrecería protección contra una amplia gama de coronavirus, independientemente de sus variantes. Esto reduciría la necesidad de modificar la vacuna de forma regular.

Hatchett describió estas vacunas como el “santo grial”. Pero argumentó que puede llevar años de inversión. Dijo: “Si quieres cultivar un árbol, lo mejor que puedes haber hecho es haberlo plantado hace 20 años. Y si no hiciste eso, lo mejor que puedes hacer es plantarlo hoy “.
Cuando se le preguntó cuál sería la mejor vacuna para tratar el Sars-CoV-2, Hatchett respondió: “En realidad, aún no lo sabemos específicamente. Este es realmente nuestro primer contacto con este virus, obviamente, y lo hemos visto expandirse y desarrollarse con el tiempo ... Todavía estamos recopilando datos y adquiriendo experiencia al respecto. Creo que debemos tener algo de humildad sobre lo que sabemos actualmente y lo que podemos saber. Solo tenemos que estar atentos.
¿Por qué está mutando el Sars-CoV-2?
Ninguno de los científicos que entrevistamos se sorprendió al ver la mutación del Sars-CoV-2. Todos los virus mutan. A menudo sufren cambios genéticos aleatorios porque la maquinaria de replicación del virus no es perfecta. Es un poco como un juego de “teléfono” donde los niños repiten lo que creyeron escuchar, cometiendo errores a lo largo del camino para que el mensaje final sea muy diferente al original. Siempre que un virus desarrolla una o más mutaciones, se considera una “variante” del virus original.
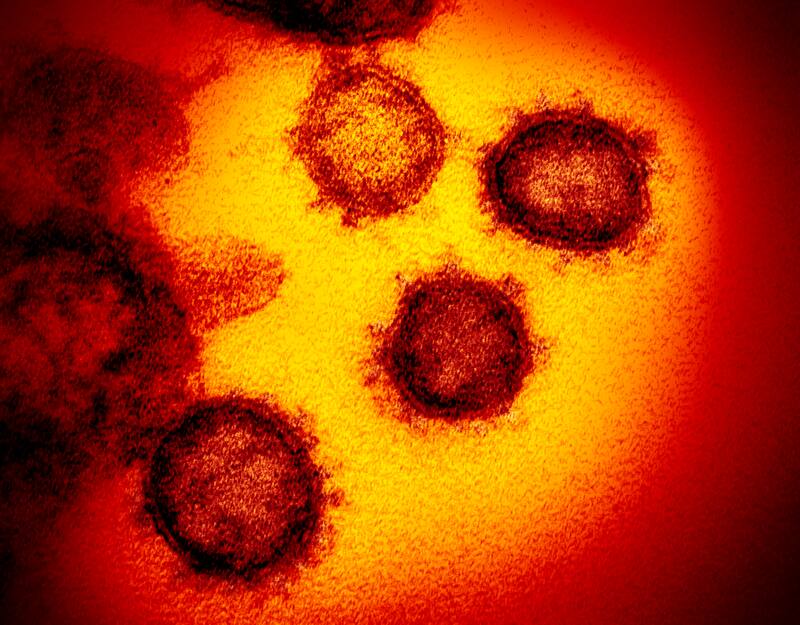
El proceso de mutación ayuda a los virus a adaptarse y sobrevivir a cualquier ataque del sistema inmunológico del huésped, la vacunación o el tratamiento con medicamentos y la competencia natural. Los virus cambian más rápido cuando están bajo tales presiones.
Los científicos han estado monitoreando las variaciones genéticas en el Sars-CoV-2 desde el comienzo de la pandemia. Lo hacen secuenciando el ARN total (genoma) del virus recolectado de muestras de pacientes. El genoma es el conjunto completo de instrucciones genéticas que un organismo necesita para funcionar y prosperar.
Los científicos en China lograron secuenciar el primer genoma del Sars-CoV-2 solo una semana después de que el primer paciente fuera hospitalizado con una neumonía inusual en Wuhan. Redactada por primera vez el 5 de enero de 2020, la secuencia reveló que el virus es un pariente cercano del Sars-CoV-1, un coronavirus humano que provocó un brote de una enfermedad respiratoria grave Sars que apareció por primera vez en China en 2002 y luego se propagó a muchos otros países. También se parecía a un coronavirus similar al Sars que se encuentra en los murciélagos.

El genoma del Sars-CoV-2, que consta de una sola hebra de ARN, resultó ser el genoma más largo de todos los virus de ARN conocidos. Con la ayuda de la secuenciación, los científicos pudieron identificar rápidamente los genes que llevan las instrucciones para la proteína de pico, la parte del virus que le ayuda a invadir las células humanas. Esto se convirtió en un objetivo importante para el desarrollo de la vacuna Covid-19.
Los datos iniciales de secuenciación del genoma sugirieron que el Sars-CoV-2 mutaba mucho más lentamente que la mayoría de los otros virus de ARN, siendo la mitad de la tasa del virus responsable de la gripe y una cuarta parte de la encontrada para el VIH. Sin embargo, su tasa de mutación ha aumentado la velocidad con el tiempo, ayudado por el gran reservorio de personas que ha infectado y presiones de selección.
No todas las mutaciones son malas noticias. En algunos casos, debilitan el virus y la variante desaparece sin dejar rastro. Pero en otros casos, permiten que el virus entre más fácilmente en las células del huésped o escape del sistema inmunológico con mayor eficacia, lo que dificulta su prevención y tratamiento.
Hasta ahora, han surgido cinco nuevas variantes preocupantes con el Sars-CoV-2. El primero (Alfa) se detectó en el sureste de Inglaterra en septiembre de 2020. Otros se encontraron poco después en Sudáfrica (Beta), Brasil (Gamma), India (Delta) y Perú (Lambda). Lo preocupante de estas nuevas variantes es que son más transmisibles, lo que hace que se propaguen más rápido, lo que aumenta la probabilidad de reinfección y resurgimiento de casos. Todos los virus Sars-CoV-2 que existen hoy en día son una variación del original y seguirán apareciendo nuevas variantes.
La investigación preliminar sugiere que la primera generación de vacunas ofrece cierta protección contra las nuevas variantes, lo que ayuda a reducir las enfermedades graves y la hospitalización. Sin embargo, probablemente se volverán menos efectivos con el tiempo a medida que el virus muta aún más y la inmunidad que las personas han ganado, ya sea a través de la vacunación o la infección natural, disminuye.
Buscando puntos débiles
En términos de una vacuna universal contra el coronavirus, la pregunta fundamental, cree Hatchett, es si existen puntos débiles que se “conservan en los coronavirus como una familia viral a la que se pueden desarrollar respuestas inmunitarias que lo protejan de manera efectiva”.
La cuestión clave en la creación de una vacuna universal es qué tan amplia debe ofrecer la vacuna. Andrew Ward también nos lo señaló en el Instituto de Investigación Scripps en California. Como él lo expresó: “¿Debería ser Sars-CoV-2 y variantes? ¿Debería ser Sars-1 y Sars-2? ¿Deberían ser todos los sarbecocovirus [un subgrupo de virus del SARS de los cuales el Sars-CoV-1 y 2 son miembros notables] o virus similares al Sars? Eso es desconocido. Sabemos que los virus del Sars existen en murciélagos y pangolines y nunca han sido un problema tan grande como ahora. Pero es una de esas cosas, que si no es realmente un problema, ¿lo perseguimos y tratamos de implementar de manera proactiva programas de vacunas y hacer que las personas se vacunen o almacenen vacunas?”

Crear una vacuna universal es en sí mismo un gran desafío. Por ejemplo, los científicos han intentado durante años, pero aún no han tenido éxito, en desarrollar una vacuna universal contra la influenza. Tampoco han logrado crear uno para el VIH. En parte, esto se debe a que las proteínas de superficie que se encuentran en estos virus cambian con frecuencia su apariencia. Esto dificulta que nuestro sistema inmunológico reconozca el virus.
Pero los científicos han logrado enormes avances en los últimos años en la comprensión de la interacción entre el sistema inmunológico y los virus que causan la gripe y el VIH. Ahora están implementando este conocimiento para construir una vacuna universal para los coronavirus, que no cambian tan rápido .
Una larga historia de innovación en vacunas
Una de las razones del optimismo con una vacuna universal contra el coronavirus es el desarrollo exitoso de la vacuna Sars-CoV-2. Fabricada en un tiempo récord, la base de la vacuna se estableció hace muchos años. Hasta la década de 1980, la mayoría de las vacunas se desarrollaban modificando un virus o una bacteria para que dejara de ser peligroso. Esto se logró debilitando o inactivando el patógeno para que pudiera inyectarse de manera segura para estimular una respuesta inmune. Si bien fue muy exitoso para proteger contra enfermedades del huésped como el sarampión, la poliomielitis, la rabia y la varicela, este enfoque no resultó efectivo en todas las enfermedades.

En la década de 1980, la producción de vacunas se encontraba en la cúspide del cambio ayudado por el surgimiento de la biotecnología. Donde esto se aplicó con éxito por primera vez fue en el desarrollo de una vacuna contra la hepatitis B, que se estima que causa más muertes en todo el mundo que la tuberculosis, el VIH o la malaria.
La primera vacuna contra la hepatitis B fue desarrollada por Maurice Hilleman en Merck. Aprobada en 1981, fue la primera vacuna para proteger contra el cáncer. La hepatitis B crónica es una de las principales causas de cáncer de hígado. De hecho, solo es superado por el tabaco como carcinógeno humano . Lo novedoso de la vacuna contra la hepatitis B fue que, en lugar de usar todo el virus de la hepatitis B, que era difícil de cultivar en el laboratorio, solo usaba una partícula del virus en la superficie de la capa . Este fue un gran avance para la tecnología de vacunas.
Otra vacuna que utiliza partículas de virus es la contra el virus del papiloma humano (VPH) que causa el cáncer de cuello uterino, una enfermedad que en todo el mundo mata a 260.000 mujeres cada año. Licenciada por primera vez en 2005, la vacuna contra el VPH tardó años en desarrollarse. Consiste en pequeñas proteínas que se parecen al exterior de cuatro tipos de VPH reales producidos en la levadura.
Vacunas sintéticas
La tecnología de las vacunas experimentó una nueva revolución tras el brote de la pandemia de gripe porcina que azotó el mundo durante 19 meses a partir de enero de 2009. La pandemia mató a entre 151.700 y 575.400 personas en todo el mundo. Causado por un virus de influenza H1N1, el episodio fue un recordatorio importante de la velocidad a la que pueden atacar las pandemias y el caos que pueden sembrar. También fue una lección saludable para las empresas que desarrollaron cientos de millones de dosis de vacunas autorizadas para contrarrestar la pandemia. Aunque se logró en solo seis meses, un récord histórico, esto no fue lo suficientemente rápido; para entonces, el pico de infecciones había pasado.

Parte del retraso se debió al tiempo necesario para que el virus creciera lo suficiente en huevos o en células cultivadas de mamíferos. Otro método, que utiliza ingeniería genética para producir el virus, resultó mucho más rápido, pero se vio obstaculizado por trabas regulatorias. Decididos a acelerar la disponibilidad de vacunas para futuras pandemias, a partir de 2011, los expertos en vacunas pusieron en marcha una nueva estrategia que aprovechó los avances en genómica y el intercambio abierto de datos de secuencias electrónicas.
Junto con una nueva capacidad para sintetizar genes, estas herramientas dieron a los científicos el poder de diseñar segmentos del genoma de un virus para preparar vacunas para entrenar al cuerpo a reconocer y atacar un virus real si lo invadía.
Fundamentalmente, el nuevo enfoque sintético alejó el desarrollo de vacunas del proceso lento de aislar y enviar virus entre diferentes sitios y luego cultivarlos a escala. Todo lo que se necesitaba era descargar los datos de secuencia relevantes de Internet y sintetizar los genes correctos para generar componentes virales relevantes para comenzar el desarrollo de la vacuna. La velocidad no era la única ventaja que ofrecía el nuevo método. También redujo cualquier riesgo potencial de riesgo biológico involucrado en la fabricación de la vacuna.
También se prestó atención a hacer más eficiente el proceso de prueba. Por lo general, la parte más lenta del desarrollo de una vacuna, son las pruebas, que suelen tardar años en completarse. Las pruebas se realizan primero en animales para evaluar la seguridad, la fuerza de la respuesta inmune estimulada y la eficacia protectora de la vacuna candidata. Una vez hecho esto, se prueba en humanos.
Los ensayos en humanos se llevan a cabo en tres fases, cada una con un número cada vez mayor de personas y costos en aumento. Una forma de reducir el tiempo necesario y reducir los costos fue aprovechar los nuevos biomarcadores. Estos proporcionaron un medio para medir tanto los procesos normales como patológicos, así como las respuestas a un fármaco. Dichos biomarcadores permitieron determinar la toxicidad y eficacia de un candidato mucho antes en el proceso de ensayo clínico y realizar múltiples ensayos en paralelo sin comprometer la seguridad.
En 2011, un grupo de científicos de las empresas Novartis y Synthetic Genomics, así como del Craig Venter Institute (una organización de investigación sin fines de lucro) demostraron que podían desarrollar una vacuna candidata en cuestión de días.
Su enfoque se puso a prueba por primera vez con éxito en marzo de 2013 cuando los funcionarios de salud chinos informaron que una nueva cepa de influenza aviar había infectado a tres personas. En solo una semana de obtener acceso a la secuencia del genoma del virus, el equipo de Novartis, encabezado por Rino Rappoli, logró crear una vacuna basada en ARN totalmente sintética lista para pruebas preclínicas, que demostró ser segura y provocó una buena respuesta inmune.
Marcando el cambio de lo que Rappouli llama “vacunas analógicas” a “vacunas digitales”, el trabajo de 2013 proporcionó una plantilla para cuando Covid-19 se declaró una pandemia el 11 de marzo de 2020. La primera dosis de la vacuna candidata Covid-19, desarrollada por Moderna, estaba lista para las pruebas de fase I en humanos el 16 de marzo de 2020 . A partir de entonces, muchos otros candidatos a vacunas pronto entraron en proceso.
Nuevos entendimientos
Lo que también ayudó a impulsar las primeras vacunas Covid-19 fue la explosión del conocimiento sobre la estructura atómica de las proteínas que se encuentran en la superficie de los virus y los anticuerpos que se unen a ellas. Según Ward, esto fue de gran ayuda gracias a los avances en la microscopía crioelectrónica que, como él dice, “abrió la puerta al VIH y otros patógenos”. Con la técnica, Ward y sus colegas descubrieron que los coronavirus entraron y se fusionaron con células humanas con la ayuda de un pequeño bucle de aminoácidos, llamado S-2P, en la parte superior de sus proteínas de pico. Esto sentó una base importante para la creación de las vacunas Covid-19.
Otro avance crítico fue el descubrimiento de anticuerpos ampliamente neutralizantes (bNAb). Aislados por primera vez a principios de la década de 1990 en el suero de personas que viven con el VIH-1, estos anticuerpos solo aparecen en algunas personas después de años de infección. Dichos anticuerpos tienen la ventaja de que pueden neutralizar múltiples cepas diversas del virus de un solo golpe.
Encontrar los bNAbs abrió críticamente una nueva vía para el diseño de vacunas. En particular, ofreció la posibilidad de crear una vacuna universal contra la gripe y también una vacuna para el VIH que hasta ahora ha sido difícil de hacer porque muta muy rápido. Varios grupos ya habían avanzado en este campo antes de que golpeara el Covid-19, que rápidamente se dirigieron hacia los coronavirus. Su objetivo era crear una vacuna para estimular la producción de bNAbs dirigidos al dominio de unión al receptor (RBD) ubicado en la proteína de pico del coronavirus.
Un enfoque, que nos describió Barton Haynes , inmunólogo de la Universidad de Duke, implica unir pequeños fragmentos del RBD, de múltiples coronavirus, a una nanopartícula de proteína para usar como candidata a vacuna. De manera prometedora, se demostró que esto en monos no solo bloquea el Sars-CoV-2 y sus nuevas variantes preocupantes, sino también el Sars-CoV-1 y un grupo de coronavirus de murciélago que podrían extenderse a los humanos en el futuro.
Otra posible vacuna fue descrito por Pamela Bjorkman, un inmunólogo estructural en el Caltech . Su equipo lo desarrolló basándose en una plataforma de partículas de virus ideada por primera vez en la Universidad de Oxford en 2016. Ella dijo: “Mi laboratorio realmente se dedica a la biología estructural, lo que significa que observamos las estructuras tridimensionales de los objetivos del sistema inmunológico, que generalmente son picos que salen del virus. Entonces, los coronavirus tienen los famosos picos, al igual que el VIH y la influenza”.

Una de las cosas que hemos estado tratando de hacer [para una vacuna] es hacer una nanopartícula, que es una pequeña cosa que parece una pelota de fútbol en miniatura. Y adjunte piezas de la púa a eso usando una tecnología muy fácil que se desarrolló en la Universidad de Oxford.
Su vacuna presenta muchos fragmentos de RBD diferentes, de una variedad de coronavirus animales, injertados en pequeñas proteínas unidas a un andamiaje de nanopartículas. Las pruebas en ratones mostraron que una sola dosis de la vacuna podría neutralizar múltiples coronavirus humanos y animales, incluidos los que no están incluidos en el diseño de la vacuna.
Según nuestra entrevista con Jonathan Heeney, patólogo comparativo de la Universidad de Cambridge, su grupo también ha desarrollado una vacuna contra el coronavirus de amplia cobertura prometedora. Sobre la base de un análisis detallado de la estructura del virus, han sintetizado construcciones de ADN para conectarlas a las plataformas de vacunas convencionales y la última tecnología de vacunas de ARNm.
El vector está especialmente diseñado para no desencadenar respuestas hiperinflamatorias involuntarias, que a veces pueden poner en peligro la vida. En estudios con animales, su candidato proporcionó protección contra una variedad de sarbecovirus, que cubren el Sars-CoV-1, el Sars-CoV-2 y muchos coronavirus de murciélago.
Los tres enfoques descritos aún no se han probado en humanos. El de Cambridge está programado para ingresar a las pruebas de fase 1 en otoño y el de la Universidad de Duke también se está acercando a ese hito. Tanto los candidatos de Cambridge como de Caltech tienen el atractivo de que pueden producirse como un polvo liofilizado y termoestable. Esto hará que su almacenamiento y distribución sea mucho más fácil que las vacunas de ARNm actuales (Moderna y Pfizer). También hará que la producción sea mucho más barata, lo cual es vital para garantizar un acceso equitativo a la vacuna en todo el mundo y controlar la pandemia.
Nuevas pandemias
Si bien los científicos tienen las herramientas para desarrollar una vacuna contra el coronavirus dentro de un año, su creación no sería el final de la historia. La creciente densidad de población, la movilidad humana y el cambio ecológico significan que el mundo seguirá enfrentando la amenaza de nuevas pandemias.

Hacer frente a este desafío requerirá un alto grado de vigilancia de brotes, voluntad política y cooperación internacional, así como una inversión continua en el desarrollo de vacunas mucho más allá del final de la pandemia de Covid-19. Como dijo la OMS en septiembre de 2020, “una pandemia mundial requiere un esfuerzo mundial para ponerle fin; ninguno de nosotros estará seguro hasta que todos estén a salvo”.
El acceso a las vacunas es también solo una parte de lo que se necesita para combatir las pandemias. Lo que también nos ha enseñado el Sars-CoV-2 es la importancia de la secuenciación genómica rápida de primera línea sobre el terreno para detectar rápidamente las amenazas emergentes. Como sostiene Hatchett, la clave para reducir radicalmente el riesgo de epidemias y pandemias en el mundo es a través de “detección más temprana, secuenciación más temprana y respuestas de salud pública más tempranas y adaptadas”.
*Investigador invitado, Historia de las Ciencias Biomédicas, Universidad de Cambridge
**Líder de grupo, Salud Global (Enfermedades Infecciosas), Universidad de Cambridge
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
Casi nadie tiene claro qué es un modelo generativo. El resto lo leyó en La Tercera
Plan Digital + LT Beneficios$6.990 al mes SUSCRÍBETE













